研究内容
急性骨髄性白血病(AML)のゲノム解析
急性骨髄性白血病(AML)は、白血球になる前の未熟な細胞の染色体や遺伝子に異常が起こり、がん化した白血病細胞が主に骨髄で無制限に増殖する疾患です。AMLは成人にみられる白血病の中で最も頻度が高いとされています。一方、小児のAMLは比較的頻度が低く、年間200名程度が発症しています。我々のグループは、日本小児がん研究グループ(JCCG)の臨床試験に登録された全国の医療機関のAML患者さんの余剰サンプルを解析し、小児AMLにみられるゲノム異常とその臨床的・機能的意義を明らかにしてきました(Blood Cancer J. 2014, Haematologica. 2014, Pediatr Blood Cancer. 2016, Pediatr Int. 2018, Blood Adv. 2018, Blood Adv. 2020, Int J Hematol. 2021, Br J Haematol. 2021, Haematologica. 2022, Blood. 2024, Leukemia. 2024, etc.)。
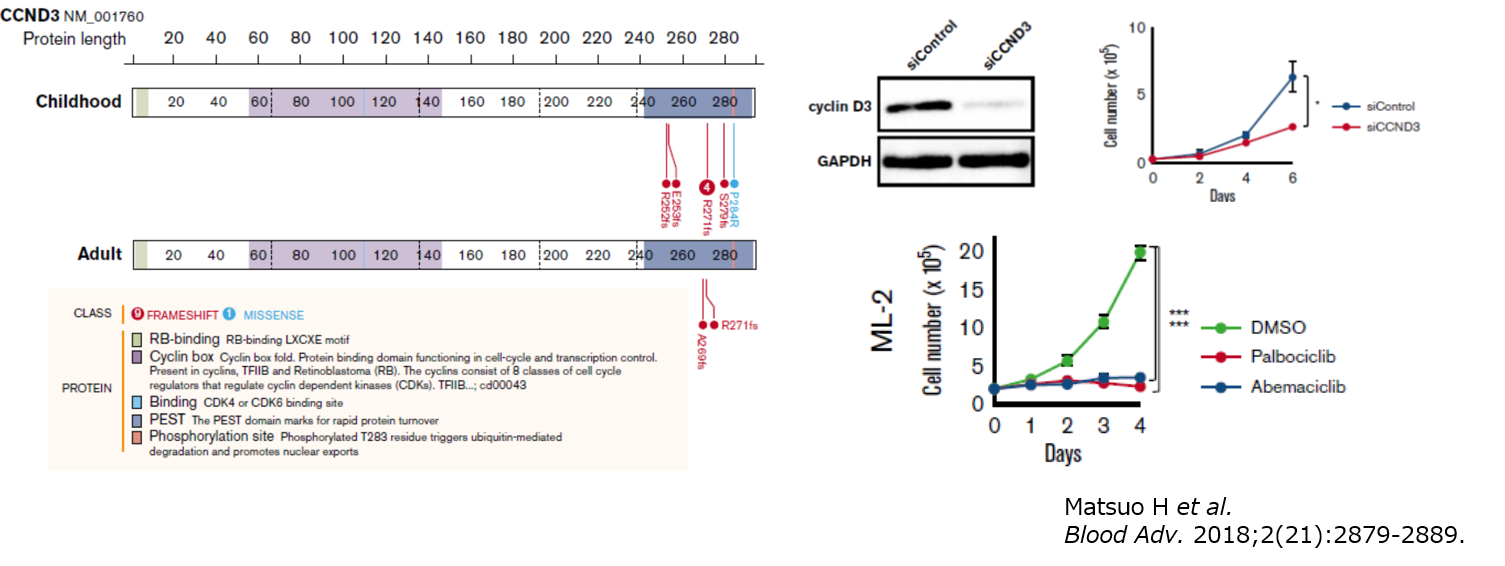
AMLには様々な病型が存在しますが、我々は乳児で特に頻度の高いKMT2A再構成という染色体異常を持つ病型に注目しています。KMT2A再構成AMLは他の病型と比較して遺伝子変異の数が少ないことが報告されていましたが、詳細な遺伝子解析は行われていませんでした。我々はKMT2A再構成AMLサンプルの次世代シークエンス解析(全エクソン解析、ターゲットシークエンス解析)により、CCND3という遺伝子変異が高頻度にみられることを明らかにしました。また、CCND3遺伝子の変異や高発現を伴うAML細胞株を用いて、乳がんで臨床応用されているCDK4/6阻害剤が有効である可能性を見出しました(Blood
Adv. 2018、日本経済新聞掲載、プレスリリース)。
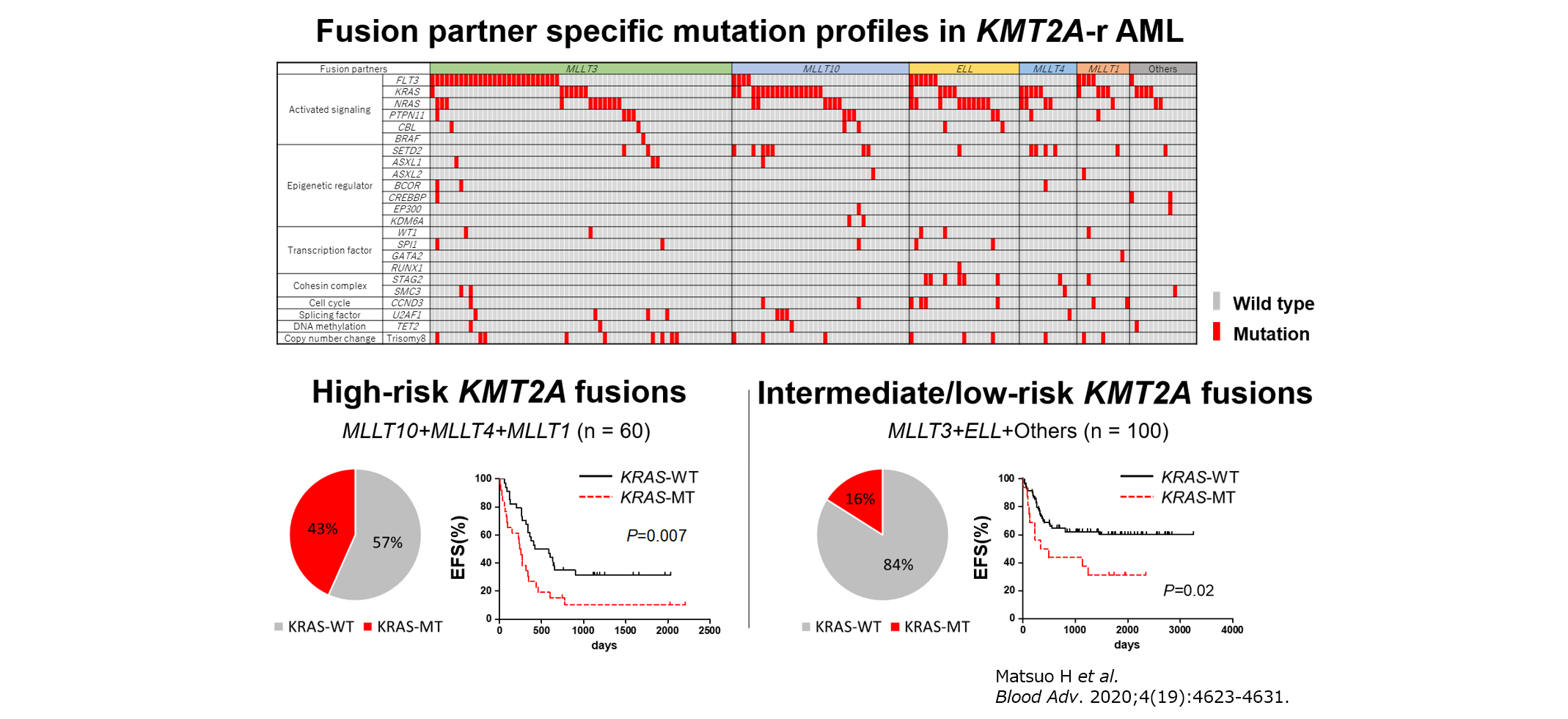
KMT2A再構成のパターンは60以上が知られ、このうち一部はAML患者の予後(治りにくさ)と関連することから治療層別化に用いられています。しかし、KMT2A再構成AMLの遺伝子異常が予後に与える影響は不明でした。そこで本邦の解析結果と海外のAML患者データセットを統合して解析し、KRAS遺伝子変異を持つ症例は予後不良であることを明らかにしました。興味深いことに、KRAS遺伝子変異は、従来予後不良とされてきたKMT2A再構成パターンを持つ症例で頻度が高く、高リスクの患者群・低~中間リスクの患者群のいずれにおいても予後不良と関連していました(Blood
Adv. 2020、プレスリリース)。
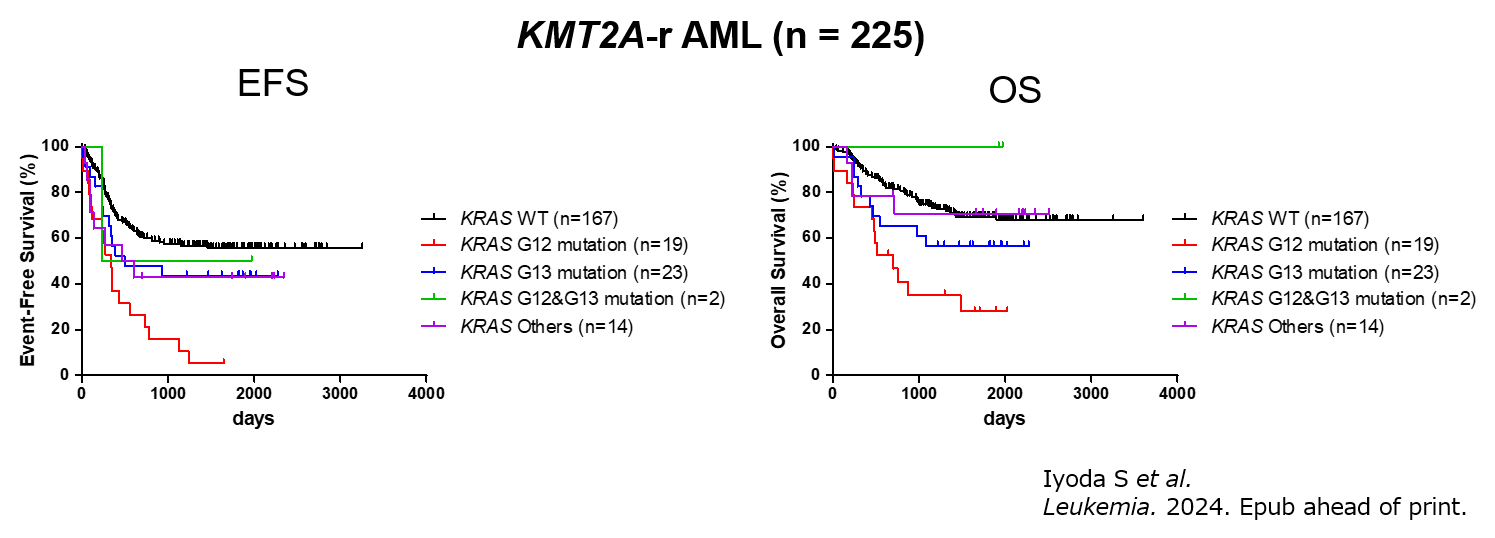
最近では、より多数の臨床検体を用いた解析により、KMT2A再構成AMLにおいてKRAS遺伝子の中でもコドン12という部位に変異を持つ症例は、他の症例と比較して予後不良であることが明らかになりました。よって、KRAS遺伝子のコドン12変異の有無を調べることで、AMLのより正確な予後予測が可能になり、リスクに応じた最適な治療につながる可能性が考えられます(Leukemia.
2024、読売新聞・日刊工業新聞掲載、プレスリリース)。
現在は、なぜ上記のゲノム異常が予後不良と関連しているかのメカニズム解析や、AMLで見つかっている他のゲノム異常の臨床的・機能的意義の解明、それに基づいたAMLの新規治療法開発に取り組んでいます。また、AML-R15臨床試験(小児急性骨髄性白血病難治例の前方視的観察研究 研究代表者:宮﨑大学
盛武先生)や、AML-P17臨床試験(新規診断小児急性前骨髄球性白血病における化学療法剤減量を目指した第II相臨床試験 研究代表者:東京都立小児総合医療センター
湯坐先生)にも参画し、AML臨床検体のゲノム解析を行っています。
さらに、新規プロジェクトとしてAMLの髄外浸潤に関わるメカニズム解析や、少量AMLサンプルからの全ゲノム解析法の確立といった新規検査技術開発も進めています。
AMLに対する新規分化誘導治療薬の開発
日本医療研究開発機構(AMED) 創薬総合支援事業 創薬ブースターの支援を受け、幅広い病型のAMLに対し新たな機序で分化誘導効果を発揮する薬剤を見出すための大規模なスクリーニングを実施しました。(プロジェクト名:「急性骨髄性白血病の新規分化誘導治療薬の探索」2021~2024年度) 2025年度からはAMED 2025年度橋渡し研究プログラム(シーズA)京都大学拠点の採択を受け、生命科学・創薬研究支援基盤事業(BINDS)の支援を受けながら、ヒット化合物の構造展開や有効性の検証を実施しています。
特許申請の関係で現時点ではホームページで詳細を開示することはできませんが、興味のある学生には所定の手続きを経てプロジェクトに関わっていただくことができます。
血液腫瘍の新規検査法開発と症例解析
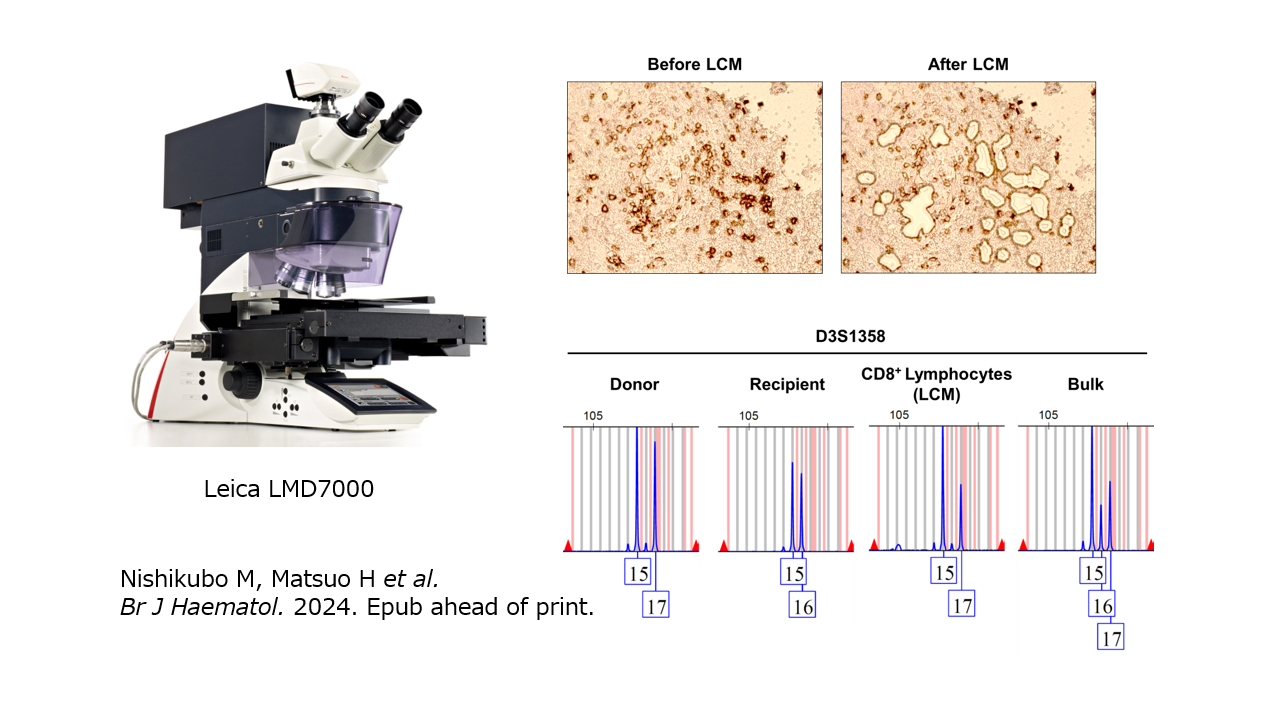
レーザーマイクロダイセクション(略称:LCM, LMDなど)はレーザー照射装置を搭載した特殊な顕微鏡で、病理標本や血液塗抹標本から顕微鏡観察下で目的細胞を採取することができます。本装置を用いたシングルセル採取や微量検体からのゲノム解析技術の確立、本技術を用いた血液腫瘍症例の詳細な病態解析に、血液内科や国立がん研究センター研究所などと共同で取り組んでいます。
最近では、脳GVHD疑い症例の脳生検組織に浸潤したリンパ球をLCMにて採取し、マイクロサテライト解析を実施することで、脳組織に浸潤したリンパ球がドナー由来であることを証明しました(Br
J Haematol. 2024、神戸市立医療センター中央市民病院 西久保先生・近藤先生、関西医科大学法医学 眞鍋先生との共同研究)。